તાજેતરમાં, માર્કેટિંગ માટે ત્રણ જીન થેરાપી દવાઓ મંજૂર કરવામાં આવી છે, જેમ કે: (1) જુલાઈ 21, 2022 ના રોજ, PTC Therapeutics, Inc. (NASDAQ: PTCT) એ જાહેરાત કરી હતી કે તેની AAV જીન થેરાપી Upstaza™ યુરોપિયન કમિશન દ્વારા મંજૂર કરવામાં આવી છે તે પ્રથમ માર્કેટિંગ જીન થેરાપી છે જે મગજમાં સીધી રીતે ઇન્જેક્ટ કરવામાં આવી હતી: અન્ય એક જીન થેરાપી (Geneene) વિશ્વના પ્રથમ લેખ. મગજમાં સીધા ઇન્જેક્ટ કરવામાં આવતી થેરાપી માર્કેટિંગ માટે મંજૂર કરવામાં આવે છે).(2) 17 ઓગસ્ટ, 2022 ના રોજ, યુએસ ફૂડ એન્ડ ડ્રગ એડમિનિસ્ટ્રેશન (FDA) એ બીટા થેલેસેમિયાની સારવાર માટે બ્લુબર્ડ બાયોની જીન થેરાપી ઝિન્ટેગ્લો (બેટીબેગ્લોજેન ઓટોટેમસેલ, બેટી-સેલ)ને મંજૂરી આપી હતી.યુનાઇટેડ સ્ટેટ્સમાં થેરાપીની મંજૂરી એ નિઃશંકપણે નાણાકીય કટોકટીમાં રહેલા બ્લુબર્ડ બાયો માટે "બરફમાં મદદ" છે.(3) ઓગસ્ટ 24, 2022 ના રોજ, BioMarin ફાર્માસ્યુટિકલ (BioMarin) એ જાહેરાત કરી કે યુરોપીયન કમિશને ROCTAVIAN™ (valoctocogene roxaparvovec), હિમોફીલિયા A માટે જીન થેરાપીના શરતી માર્કેટિંગને મંજૂરી આપી છે, જે દર્દીઓની સારવાર માટે FVIII ફેક્ટર ઇન્હિબિટર્સનો ઇતિહાસ ધરાવતા નથી અને એટીએમએવી એડલ્ટ એડલ્ટ એડલ્ટ હેમોફિલિઆ એ. બાયોમેરિનની હિમોફિલિયા એ જનીન ઉપચાર માર્કેટિંગ માટે મંજૂર).અત્યાર સુધીમાં, 41 જીન થેરાપી દવાઓ વિશ્વભરમાં માર્કેટિંગ માટે મંજૂર કરવામાં આવી છે.
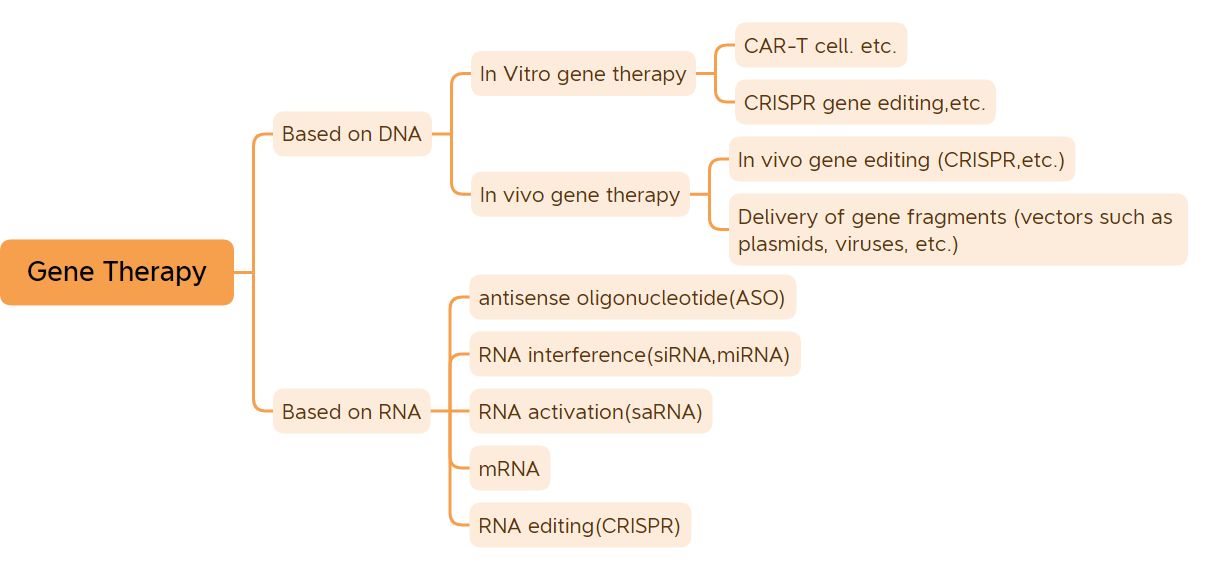
જનીન એ મૂળભૂત આનુવંશિક એકમ છે જે લક્ષણોને નિયંત્રિત કરે છે.કેટલાક વાયરસના જનીનો સિવાય, જે આરએનએથી બનેલા હોય છે, મોટાભાગના સજીવોના જનીનો ડીએનએથી બનેલા હોય છે.જીવતંત્રના મોટા ભાગના રોગો જનીનો અને પર્યાવરણ વચ્ચેની ક્રિયાપ્રતિક્રિયાને કારણે થાય છે, અને ઘણા રોગોને જીન થેરાપી દ્વારા સારમાં અથવા દૂર કરી શકાય છે.જીન થેરાપીને દવા અને ફાર્મસી ક્ષેત્રે એક ક્રાંતિ માનવામાં આવે છે.વ્યાપક જીન થેરાપી દવાઓમાં ડીએનએ-સંશોધિત ડીએનએ દવાઓ (જેમ કે વિવો જીન થેરાપી દવાઓમાં વાયરલ વેક્ટર-આધારિત, વિટ્રો જીન થેરાપી દવાઓ, નેકેડ પ્લાઝમિડ દવાઓ, વગેરે) અને આરએનએ દવાઓ (જેમ કે એન્ટિસેન્સ ઓલિગોન્યુક્લિયોટાઇડ દવાઓ, અને એમઆરએનએ, એમઆરએનએ દવાઓ, વગેરે) પર આધારિત દવાઓનો સમાવેશ થાય છે.સંકુચિત રીતે વ્યાખ્યાયિત જીન થેરાપી દવાઓમાં મુખ્યત્વે પ્લાઝમિડ ડીએનએ દવાઓ, વાયરલ વેક્ટર પર આધારિત જીન થેરાપી દવાઓ, બેક્ટેરિયલ વેક્ટર પર આધારિત જીન થેરાપી દવાઓ, જીન એડિટિંગ સિસ્ટમ્સ અને સેલ થેરાપી દવાઓનો સમાવેશ થાય છે જે વિટ્રોમાં આનુવંશિક રીતે સંશોધિત થાય છે.વર્ષોના કઠોર વિકાસ પછી, જનીન ઉપચાર દવાઓએ પ્રેરણાદાયી ક્લિનિકલ પરિણામો પ્રાપ્ત કર્યા છે.(DNA રસીઓ અને mRNA રસીઓ સિવાય), 41 જીન થેરાપી દવાઓ વિશ્વમાં માર્કેટિંગ માટે મંજૂર કરવામાં આવી છે.ઉત્પાદનોની શરૂઆત અને જનીન ઉપચાર તકનીકના ઝડપી વિકાસ સાથે, જનીન ઉપચાર ઝડપી વિકાસના સમયગાળાની શરૂઆત કરવા જઈ રહી છે.
જનીન ઉપચારનું વર્ગીકરણ (છબી સ્ત્રોત: જૈવિક જિંગવેઈ)
આ લેખ 41 જનીન ઉપચારની યાદી આપે છે જેને માર્કેટિંગ માટે મંજૂર કરવામાં આવી છે (DNA રસીઓ અને mRNA રસીઓ સિવાય).
1. ઇન વિટ્રો જીન થેરાપી
(1) સ્ટ્રિમવેલિસ
કંપની: ગ્લેક્સોસ્મિથક્લાઇન (GSK) દ્વારા વિકસિત.
બજાર માટે સમય: મે 2016 માં યુરોપિયન યુનિયન દ્વારા મંજૂર.
સંકેતો: ગંભીર સંયુક્ત ઇમ્યુનોડેફિસિયન્સી (SCID) ની સારવાર માટે.
ટિપ્પણીઓ: આ ઉપચારની સામાન્ય પ્રક્રિયા એ છે કે પ્રથમ દર્દીના પોતાના હિમેટોપોએટિક સ્ટેમ કોષો મેળવવા, તેમને વિટ્રોમાં વિસ્તૃત અને સંવર્ધન કરવા, અને પછી તેમના હેમેટોપોએટિક સ્ટેમ કોશિકાઓમાં કાર્યાત્મક ADA (એડેનોસિન ડીમિનેઝ) જનીનની નકલ દાખલ કરવા માટે રેટ્રોવાયરસનો ઉપયોગ કરવો, અને અંતે સંશોધિત હિમેટોપોએટિક સ્ટેમ કોષોને સ્થાનાંતરિત કરવું.હેમેટોપોએટીક સ્ટેમ કોશિકાઓ શરીરમાં પાછી ભેળવવામાં આવે છે.ક્લિનિકલ પરિણામો દર્શાવે છે કે સ્ટ્રિમવેલિસ સાથે સારવાર કરાયેલા ADA-SCID દર્દીઓનો 3-વર્ષનો જીવિત રહેવાનો દર 100% હતો.
(2) ઝાલ્મોક્સિસ
કંપની: મોલમેડ, ઇટાલી દ્વારા ઉત્પાદિત.
બજાર માટે સમય: 2016 માં EU શરતી માર્કેટિંગ અધિકૃતતા પ્રાપ્ત કરી.
સંકેતો: તેનો ઉપયોગ હેમેટોપોએટીક સ્ટેમ સેલ ટ્રાન્સપ્લાન્ટેશન પછી દર્દીઓની રોગપ્રતિકારક શક્તિના સહાયક ઉપચાર માટે થાય છે.
રિમાર્કસ: ઝાલ્મોક્સિસ એ એલોજેનિક ટી સેલ સ્યુસાઇડ જનીન ઇમ્યુનોથેરાપી છે જે રેટ્રોવાયરલ વેક્ટર દ્વારા સુધારેલ છે.1NGFR અને HSV-TK Mut2 આત્મઘાતી જનીનો લોકોને કોઈપણ સમયે ganciclovir નો ઉપયોગ કરવાની મંજૂરી આપે છે જેથી પ્રતિકૂળ રોગપ્રતિકારક પ્રતિક્રિયાઓનું કારણ બને તેવા T કોષોને મારવા, GVHD ના વધુ બગાડને અટકાવવા અને સર્જરી એસ્કોર્ટ પછી હેપ્લોઇડેન્ટિકલ HSCT ધરાવતા દર્દીઓમાં રોગપ્રતિકારક કાર્ય પુનઃસ્થાપિત કરવામાં આવે.
(3) ઇન્વોસા-કે
કંપની: TissueGene (KolonTissueGene) કંપની દ્વારા વિકસિત.
માર્કેટ માટેનો સમય: જુલાઈ 2017માં દક્ષિણ કોરિયામાં લિસ્ટિંગ માટે મંજૂર.
સંકેતો: ડીજનરેટિવ ઘૂંટણની સંધિવાની સારવાર માટે.
રિમાર્કસ: ઇન્વોસા-કે એ એલોજેનિક સેલ જીન થેરાપી છે જેમાં માનવ ચૉન્ડ્રોસાઇટ્સનો સમાવેશ થાય છે.એલોજેનિક કોષો વિટ્રોમાં આનુવંશિક રીતે સંશોધિત થાય છે, અને સંશોધિત કોષો ઇન્ટ્રા-આર્ટિક્યુલર ઇન્જેક્શન પછી ટ્રાન્સફોર્મિંગ ગ્રોથ ફેક્ટર β1 (TGF-β1) ને વ્યક્ત અને સ્ત્રાવ કરી શકે છે.β1), ત્યાં અસ્થિવાનાં લક્ષણોમાં સુધારો કરે છે.ક્લિનિકલ પરિણામો દર્શાવે છે કે Invossa-K ઘૂંટણની સંધિવાને નોંધપાત્ર રીતે સુધારી શકે છે.2019 માં દક્ષિણ કોરિયાના ડ્રગ રેગ્યુલેટર દ્વારા લાઇસન્સ રદ કરવામાં આવ્યું હતું કારણ કે ઉત્પાદકે ઉપયોગમાં લેવાતા ઘટકોને ખોટી રીતે લેબલ કર્યું હતું.
(4) Zynteglo
કંપની: અમેરિકન બ્લુબર્ડ બાયો (બ્લુબર્ડ બાયો) કંપની દ્વારા વિકસિત.
માર્કેટ માટેનો સમય: 2019માં યુરોપિયન યુનિયન દ્વારા મંજૂર કરવામાં આવ્યો અને ઓગસ્ટ 2022માં FDA દ્વારા મંજૂર કરવામાં આવ્યો.
સંકેતો: ટ્રાન્સફ્યુઝન આધારિત β-થેલેસેમિયાની સારવાર માટે.
રિમાર્કસ: ઝિન્ટેગ્લો એ લેન્ટીવાયરલ ઇન વિટ્રો જીન થેરાપી છે, જે દર્દીઓમાંથી દૂર કરવામાં આવેલા હેમેટોપોએટીક સ્ટેમ સેલ્સમાં સામાન્ય β-ગ્લોબિન જનીન (βA-T87Q-ગ્લોબિન જનીન) ની કાર્યાત્મક નકલ દાખલ કરવા માટે લેન્ટીવાયરલ વેક્ટરનો ઉપયોગ કરે છે., અને પછી આ આનુવંશિક રીતે સંશોધિત ઓટોલોગસ હેમેટોપોએટીક સ્ટેમ કોશિકાઓને દર્દીમાં પાછું દાખલ કરો.એકવાર દર્દી પાસે સામાન્ય βA-T87Q-ગ્લોબિન જનીન હોય, તો તેઓ સામાન્ય HbAT87Q પ્રોટીન ઉત્પન્ન કરી શકે છે, જે રક્ત તબદિલીની જરૂરિયાતને અસરકારક રીતે ઘટાડી અથવા દૂર કરી શકે છે.તે 12 વર્ષ અને તેથી વધુ ઉંમરના દર્દીઓ માટે આજીવન રક્ત તબદિલી અને આજીવન દવાઓને બદલવા માટે રચાયેલ એક વખતની ઉપચાર છે.
(5) સ્કાયસોના
કંપની: અમેરિકન બ્લુબર્ડ બાયો (બ્લુબર્ડ બાયો) કંપની દ્વારા વિકસિત.
માર્કેટિંગ માટેનો સમય: જુલાઈ 2021 માં માર્કેટિંગ માટે EU દ્વારા મંજૂર.
સંકેતો: પ્રારંભિક સેરેબ્રલ એડ્રેનોલ્યુકોડિસ્ટ્રોફી (CALD) ની સારવાર માટે.
રિમાર્કસ: સ્કાયસોના જીન થેરાપી એ પ્રારંભિક સેરેબ્રલ એડ્રેનોલ્યુકોડિસ્ટ્રોફી (CALD) ની સારવાર માટે મંજૂર કરાયેલી એકમાત્ર જનીન ઉપચાર છે.સ્કાયસોના (એલિવાલ્ડોજેન ઓટોટેમસેલ, લેન્ટી-ડી) એ વિટ્રો જીન થેરાપી લેન્ટી-ડીમાં હેમેટોપોએટીક સ્ટેમ સેલ લેન્ટીવાયરલ છે.ઉપચારની સામાન્ય પ્રક્રિયા નીચે મુજબ છે: દર્દીમાંથી ઓટોલોગસ હેમેટોપોએટીક સ્ટેમ સેલ લેવામાં આવે છે, માનવ ABCD1 જનીન વહન કરતા લેન્ટીવાયરસ દ્વારા વિટ્રોમાં સંશોધિત કરવામાં આવે છે, અને પછી દર્દીમાં પાછા દાખલ કરવામાં આવે છે.ABCD1 જીન મ્યુટેશન અને CALD સાથે 18 વર્ષથી ઓછી ઉંમરના દર્દીઓની સારવાર માટે.
(6) Kymriah
કંપની: નોવાર્ટિસ દ્વારા વિકસિત.
માર્કેટ માટેનો સમય: ઓગસ્ટ 2017 માં FDA દ્વારા મંજૂર.
સંકેતો: પૂર્વવર્તી બી-સેલ એક્યુટ લિમ્ફોબ્લાસ્ટિક લ્યુકેમિયા (ALL) અને રિલેપ્સ્ડ અને રિફ્રેક્ટરી DLBCL ની સારવાર.
રિમાર્કસ: કિમરિયા એ લેન્ટીવાયરલ ઇન વિટ્રો જીન થેરાપી દવા છે, જે વિશ્વની પ્રથમ માન્ય CAR-T થેરાપી છે, જે CD19 ને લક્ષ્ય બનાવે છે અને સહ-ઉત્તેજક પરિબળ 4-1BB નો ઉપયોગ કરે છે.યુએસમાં કિંમત $475,000 અને જાપાનમાં $313,000 છે.
(7) યસકાર્ટા
કંપની: કાઈટ ફાર્મા દ્વારા વિકસિત, ગિલિયડની પેટાકંપની.
માર્કેટ માટેનો સમય: ઓક્ટોબર 2017 માં FDA દ્વારા મંજૂર.
સંકેતો: રિલેપ્સ્ડ અથવા રીફ્રેક્ટરી મોટા બી-સેલ લિમ્ફોમાની સારવાર માટે.
રિમાર્કસ: યસકાર્ટા એ વિટ્રો જીન થેરાપીમાં રેટ્રોવાયરલ છે.તે વિશ્વમાં મંજૂર કરાયેલી બીજી CAR-T થેરાપી છે.તે CD19 ને લક્ષ્ય બનાવે છે અને CD28 ના કોસ્ટિમ્યુલેટરી ફેક્ટરનો ઉપયોગ કરે છે.યુએસમાં કિંમત $373,000 છે.
(8) ટેકાર્ટસ
કંપની: ગિલિયડ (GILD) દ્વારા વિકસિત.
બજાર માટેનો સમય: જુલાઈ 2020 માં FDA દ્વારા મંજૂર.
સંકેતો: રિલેપ્સ્ડ અથવા રિફ્રેક્ટરી મેન્ટલ સેલ લિમ્ફોમા માટે.
ટીકાર્ટસ એ CD19 ને લક્ષ્યાંકિત કરતી ઓટોલોગસ CAR-T સેલ થેરાપી છે, અને વિશ્વમાં માર્કેટિંગ માટે મંજૂર કરાયેલી ત્રીજી CAR-T થેરાપી છે.
(9) બ્રેયાંઝી
કંપની: બ્રિસ્ટોલ-માયર્સ સ્ક્વિબ (BMS) દ્વારા વિકસિત.
માર્કેટ માટેનો સમય: ફેબ્રુઆરી 2021 માં FDA દ્વારા મંજૂર.
સંકેતો: રિલેપ્સ્ડ અથવા રિફ્રેક્ટરી (R/R) લાર્જ બી-સેલ લિમ્ફોમા (LBCL).
રિમાર્કસ: બ્રેયાંઝી એ લેન્ટીવાયરસ પર આધારિત એક ઇન-વિટ્રો જીન થેરાપી છે, અને CD19 ને લક્ષ્યાંકિત કરીને વિશ્વમાં માર્કેટિંગ માટે મંજૂર કરાયેલ ચોથી CAR-T થેરાપી છે.બ્રેયાંઝીની મંજૂરી એ સેલ્યુલર ઇમ્યુનોથેરાપીના ક્ષેત્રમાં બ્રિસ્ટોલ-માયર્સ સ્ક્વિબ માટે એક સીમાચિહ્નરૂપ છે, જે બ્રિસ્ટોલ-માયર્સે જ્યારે 2019માં $74 બિલિયનમાં સેલજેન હસ્તગત કર્યું ત્યારે હસ્તગત કરી હતી.
(10) એબેકમા
કંપની: Bristol-Myers Squibb (BMS) અને બ્લુબર્ડ બાયો દ્વારા સહ-વિકસિત.
બજાર માટેનો સમય: માર્ચ 2021 માં FDA દ્વારા મંજૂર.
સંકેતો: રિલેપ્સ્ડ અથવા રિફ્રેક્ટરી મલ્ટિપલ માયલોમા.
રિમાર્કસ: એબેકમા એ લેન્ટીવાયરસ-આધારિત ઈન વિટ્રો જીન થેરાપી છે, વિશ્વની પ્રથમ CAR-T સેલ થેરાપી જે BCMA ને લક્ષ્યાંકિત કરે છે, અને FDA દ્વારા મંજૂર કરાયેલ પાંચમી CAR-T થેરાપી છે.દવાનો સિદ્ધાંત દર્દીના ઓટોલોગસ ટી કોશિકાઓ પર વિટ્રોમાં લેન્ટીવાયરસ-મધ્યસ્થી આનુવંશિક ફેરફાર દ્વારા કાઇમરિક BCMA રીસેપ્ટરને વ્યક્ત કરવાનો છે.સેલ જીન દવાના પ્રેરણા પહેલાં, દર્દીને પૂર્વ-સારવાર માટે સાયક્લોફોસ્ફામાઇડ અને ફ્લુડારાબીનના બે સંયોજનો પ્રાપ્ત થયા.દર્દીમાંથી બિનસંશોધિત ટી કોશિકાઓને દૂર કરવા માટે સારવાર, અને પછી BCMA- વ્યક્ત કરતા કેન્સર કોષોને શોધવા અને મારવા માટે દર્દીના શરીરમાં પાછા સંશોધિત ટી કોશિકાઓ દાખલ કરો.
(11) લિબમેલ્ડી
કંપની: ઓર્ચાર્ડ થેરાપ્યુટિક્સ દ્વારા વિકસિત.
બજાર માટેનો સમય: ડિસેમ્બર 2020 માં સૂચિબદ્ધ કરવા માટે યુરોપિયન યુનિયન દ્વારા મંજૂર.
સંકેતો: મેટાક્રોમેટિક લ્યુકોડિસ્ટ્રોફી (MLD) ની સારવાર માટે.
રિમાર્કસ: લિબમેલ્ડી એ ઓટોલોગસ CD34+ કોષોના લેન્ટીવાયરલ ઇન વિટ્રો જનીન ફેરફાર પર આધારિત જનીન ઉપચાર છે.ક્લિનિકલ ડેટા દર્શાવે છે કે લિબમેલ્ડીનું એક જ ઇન્ટ્રાવેનસ ઇન્ફ્યુઝન એ જ ઉંમરના સારવાર ન કરાયેલ દર્દીઓમાં પ્રારંભિક-પ્રારંભિક એમએલડી અને ગંભીર મોટર અને જ્ઞાનાત્મક ક્ષતિના કોર્સને સુધારવામાં અસરકારક છે.
(12) બેનોડા
કંપની: WuXi Junuo દ્વારા વિકસિત.
માર્કેટ માટેનો સમય: સપ્ટેમ્બર 2021માં NMPA દ્વારા અધિકૃત રીતે મંજૂર.
સંકેતો: બીજી લાઇન અથવા વધુ પ્રણાલીગત ઉપચાર પછી પુખ્ત દર્દીઓમાં રિલેપ્સ્ડ અથવા રિફ્રેક્ટરી લાર્જ બી-સેલ લિમ્ફોમા (r/r LBCL) ની સારવાર.
ટિપ્પણી: બેનોડા એ CD19 વિરોધી CAR-T જનીન ઉપચાર છે, અને તે WuXi Junuoનું મુખ્ય ઉત્પાદન પણ છે.રિલેપ્સ્ડ/રીફ્રેક્ટરી લાર્જ બી-સેલ લિમ્ફોમા સિવાય, તે ચીનમાં મંજૂર કરાયેલ બીજું CAR-T ઉત્પાદન છે.આ ઉપરાંત, WuXi Junuo એ ફોલિક્યુલર લિમ્ફોમા (FL), મેન્ટલ સેલ લિમ્ફોમા (MCL), ક્રોનિક લિમ્ફોસાયટીક લ્યુકેમિયા (CLL), સેકન્ડ-લાઈન ડિફ્યુઝ લાર્જ બી-સેલ લિમ્ફોમા (એએલડીએલબીસીએલ લિમ્ફોમા) અને એએલબીસીએલ્યુટીકમિયા (એએલડીએલયુટી) સહિત અન્ય વિવિધ સંકેતોની સારવાર માટે રુકી ઓરેન્ઝા ઈન્જેક્શન વિકસાવવાની પણ યોજના બનાવી છે.
(13) CARVYKTI
કંપની: લિજેન્ડ બાયોની પ્રથમ માન્ય પ્રોડક્ટ.
માર્કેટ માટેનો સમય: ફેબ્રુઆરી 2022 માં FDA દ્વારા મંજૂર.
સંકેતો: રિલેપ્સ્ડ અથવા રિફ્રેક્ટરી મલ્ટિપલ માયલોમા (R/R MM) ની સારવાર.
રિમાર્કસ: CARVYKTI (સિલટાકેબટેજીન ઓટોલ્યુસેલ, જેને Cilta-cel તરીકે ઓળખવામાં આવે છે) એ CAR-T સેલ ઇમ્યુન જીન થેરાપી છે જેમાં B સેલ પરિપક્વતા એન્ટિજેન (BCMA) ને લક્ષ્યાંકિત કરતી બે સિંગલ-ડોમેન એન્ટિબોડીઝ છે.ડેટા દર્શાવે છે કે CARVYKTI એ રિલેપ્સ્ડ અથવા રિફ્રેક્ટરી મલ્ટિપલ માયલોમા ધરાવતા દર્દીઓમાં 98% સુધીનો એકંદર પ્રતિભાવ દર દર્શાવ્યો હતો જેમણે પ્રોટીઝોમ ઇન્હિબિટર્સ, ઇમ્યુનોમોડ્યુલેટર્સ અને એન્ટિ-સીડી38 મોનોક્લોનલ એન્ટિબોડીઝ સહિત ચાર કે તેથી વધુ પૂર્વ ઉપચારો મેળવ્યા હતા.
2. વાયરલ વેક્ટર પર આધારિત વિવો જીન થેરાપીમાં
(1) જાતિ/પુનઃજન્મ
કંપની: શેનઝેન સાયબૈનુઓ કંપની દ્વારા વિકસિત.
માર્કેટ માટેનો સમય: 2003માં ચીનમાં લિસ્ટિંગ માટે મંજૂર.
સંકેતો: માથા અને ગરદનના સ્ક્વામસ સેલ કાર્સિનોમાની સારવાર માટે.
રિમાર્કસ: રિકોમ્બિનન્ટ હ્યુમન p53 એડેનોવાયરસ ઈન્જેક્શન જેન્ડિસિન/જિનશેંગશેંગ એ શેનઝેન સાઈબાઈનુઓ કંપનીની માલિકીના સ્વતંત્ર બૌદ્ધિક સંપદા અધિકારો સાથેની એડિનોવાઈરસ વેક્ટર જનીન ઉપચાર દવા છે.દવા સામાન્ય માનવ ટ્યુમર સપ્રેસર જનીન p53 અને કૃત્રિમ રીતે સંશોધિત રિકોમ્બિનન્ટ પ્રતિકૃતિ-ઉણપથી બનેલી છે માનવ એડેનોવાયરસ પ્રકાર 5 માનવ એડેનોવાયરસ પ્રકાર 5 થી બનેલું છે. ભૂતપૂર્વ એ એન્ટિ-ટ્યુમર અસર લાગુ કરવા માટે દવાનું મુખ્ય માળખું છે, અને બાદમાં મુખ્યત્વે કેરીર તરીકે કાર્ય કરે છે.એડેનોવાયરસ વેક્ટર રોગનિવારક જનીન p53 ને લક્ષ્ય કોષમાં વહન કરે છે, અને લક્ષ્ય કોષમાં ટ્યુમર સપ્રેસર જનીન p53 વ્યક્ત કરે છે.ઉત્પાદન વિવિધ કેન્સર વિરોધી જનીનોને ઉપર-નિયમિત કરી શકે છે અને વિવિધ ઓન્કોજીન્સની પ્રવૃત્તિઓને ડાઉન-રેગ્યુલેટ કરી શકે છે, જેનાથી શરીરની ગાંઠ-વિરોધી અસરમાં વધારો થાય છે અને ગાંઠોને મારવાના હેતુને પ્રાપ્ત થાય છે.
(2) ઋગ્વીર
કંપની: લાતવિયન કંપની લાતિમા દ્વારા વિકસિત.
બજાર માટે સમય: 2004 માં લાતવિયામાં મંજૂર.
સંકેતો: મેલાનોમાની સારવાર માટે.
રિમાર્કસ: રિગ્વીર એ જનીન-સંશોધિત ECHO-7 એન્ટરવાયરસ વેક્ટર પર આધારિત જનીન ઉપચાર છે, જેનો ઉપયોગ લાતવિયા, એસ્ટોનિયા, પોલેન્ડ, આર્મેનિયા, બેલારુસ અને અન્ય સ્થળોએ કરવામાં આવ્યો છે, અને યુરોપિયન યુનિયનના EMA સાથે પણ નોંધાયેલ છે..છેલ્લા દસ વર્ષમાં ક્લિનિકલ કેસોએ સાબિત કર્યું છે કે રિગ્વીર ઓન્કોલિટીક વાયરસ સલામત અને અસરકારક છે અને મેલાનોમાના દર્દીઓના જીવિત રહેવાના દરમાં 4-6 ગણો વધારો કરી શકે છે.આ ઉપરાંત, આ થેરાપી કોલોરેક્ટલ કેન્સર, સ્વાદુપિંડનું કેન્સર, મૂત્રાશયનું કેન્સર સહિત અન્ય વિવિધ પ્રકારના કેન્સર માટે પણ યોગ્ય છે.કેન્સર, કિડની કેન્સર, પ્રોસ્ટેટ કેન્સર, ફેફસાંનું કેન્સર, ગર્ભાશયનું કેન્સર, લિમ્ફોસારકોમા, વગેરે.
(3) ઓન્કોરીન/અંકેરુઈ
કંપની: Shanghai Sunway Biotechnology Co., Ltd દ્વારા વિકસિત.
માર્કેટ માટેનો સમય: 2005માં ચીનમાં લિસ્ટિંગ માટે મંજૂર.
સંકેતો: માથા અને ગરદનની ગાંઠ, લીવર કેન્સર, સ્વાદુપિંડનું કેન્સર, સર્વાઇકલ કેન્સર અને અન્ય કેન્સરની સારવાર.
રિમાર્કસ: ઓન્કોરીન એ ઓન્કોલિટીક વાયરસ જનીન ઉપચાર ઉત્પાદન છે જે એડેનોવાયરસને વેક્ટર તરીકે ઉપયોગ કરે છે.મેળવેલ ઓન્કોલિટીક એડેનોવાયરસ ખાસ કરીને ગાંઠોમાં અછત અથવા અસાધારણ p53 જનીનની નકલ કરી શકે છે, જે ટ્યુમર સેલ લિસિસનું કારણ બને છે, જેનાથી ગાંઠ કોષોને મારી નાખે છે.સામાન્ય કોષોને નુકસાન પહોંચાડ્યા વિના.ક્લિનિકલ પરિણામો દર્શાવે છે કે અંકે રુઈ વિવિધ પ્રકારના જીવલેણ ગાંઠો માટે સારી સલામતી અને અસરકારકતા ધરાવે છે.
(4) Glybera
કંપની: યુનિક્યુર દ્વારા વિકસિત.
બજાર માટે સમય: 2012 માં યુરોપમાં મંજૂર.
સંકેતો: લિપોપ્રોટીન લિપેઝની ઉણપ (LPLD) ની સારવાર સખત રીતે પ્રતિબંધિત ચરબીયુક્ત આહાર હોવા છતાં સ્વાદુપિંડના ગંભીર અથવા પુનરાવર્તિત એપિસોડ સાથે.
રિમાર્કસ: ગ્લાયબેરા (એલિપોજીન ટિપરવોવેક) એ વેક્ટર તરીકે AAV પર આધારિત જનીન ઉપચાર દવા છે.આ થેરાપી એએવીનો ઉપયોગ વેક્ટર તરીકે ઉપચારાત્મક જનીન LPL ને સ્નાયુ કોશિકાઓમાં સ્થાનાંતરિત કરવા માટે કરે છે, જેથી સંબંધિત કોષો લિપોપ્રોટીન લિપેઝની ચોક્કસ માત્રા ઉત્પન્ન કરી શકે, તે રોગને દૂર કરવામાં ભૂમિકા ભજવે છે, અને આ ઉપચાર એક વહીવટ પછી લાંબા સમય સુધી અસરકારક છે (અસર ઘણા વર્ષો સુધી ટકી શકે છે).દવાને 2017 માં ડીલિસ્ટ કરવામાં આવી હતી, અને તેના ડિલિસ્ટિંગના કારણો બે પરિબળો સાથે સંબંધિત હોઈ શકે છે: ખૂબ ઊંચી કિંમત અને મર્યાદિત બજાર માંગ.દવાની એક સારવારનો સરેરાશ ખર્ચ 1 મિલિયન યુએસ ડોલર જેટલો ઊંચો છે, અને અત્યાર સુધી માત્ર એક દર્દીએ તેને ખરીદી અને તેનો ઉપયોગ કર્યો છે.તબીબી વીમા કંપનીએ તેને 900,000 યુએસ ડોલરમાં ભરપાઈ કરી હોવા છતાં, તે વીમા કંપની માટે પણ મોટો બોજ છે.વધુમાં, દવા માટેનો સંકેત ખૂબ જ દુર્લભ છે, જેમાં 1 મિલિયનમાં લગભગ 1 ની ઘટના દર અને ખોટા નિદાનનો ઉચ્ચ દર છે.
(5) ઇમ્લિજિક
કંપની: એમજેન દ્વારા વિકસિત.
બજાર માટેનો સમય: 2015 માં, તેને યુનાઇટેડ સ્ટેટ્સ અને યુરોપિયન યુનિયનમાં સૂચિબદ્ધ કરવા માટે મંજૂરી આપવામાં આવી હતી.
સંકેતો: મેલાનોમા જખમની સારવાર કે જે શસ્ત્રક્રિયા દ્વારા સંપૂર્ણપણે દૂર કરી શકાતી નથી.
રિમાર્કસ: ઇમલિજિક એ આનુવંશિક રીતે સંશોધિત છે (તેના ICP34.5 અને ICP47 જનીન ટુકડાઓને કાઢી નાખવું, અને માનવ ગ્રાન્યુલોસાઇટ-મેક્રોફેજ કોલોની-ઉત્તેજક પરિબળ જીએમ-સીએસએફ જનીનને વાયરસમાં દાખલ કરવું) એટેન્યુએટેડ હર્પીસ સિમ્પ્લેક્સ વાયરસ પ્રકાર 1 (એચએસવી-1, એચએસવી-1 વાયરસ, એચએસવી-1 વાયરસ) પર એટેન્યુએટેડ હર્પીસ સિમ્પ્લેક્સ વાયરસ છે. .વહીવટની પદ્ધતિ ઇન્ટ્રાલેસનલ ઇન્જેક્શન છે.મેલાનોમાના જખમમાં ડાયરેક્ટ ઇન્જેક્શન ટ્યુમર કોશિકાઓના ભંગાણનું કારણ બની શકે છે અને ગાંઠ-વિરોધી પ્રતિરક્ષા પ્રતિભાવોને પ્રોત્સાહન આપવા માટે ગાંઠમાંથી મેળવેલા એન્ટિજેન્સ અને GM-CSF મુક્ત કરે છે.
(6) Luxturna
કંપની: સ્પાર્ક થેરાપ્યુટિક્સ દ્વારા વિકસિત, રોચેની પેટાકંપની.
માર્કેટ માટેનો સમય: 2017માં FDA દ્વારા મંજૂર કરવામાં આવ્યો અને પછી 2018માં યુરોપમાં માર્કેટિંગ માટે મંજૂર કરવામાં આવ્યો.
સંકેતો: RPE65 જનીનની ડબલ કોપીમાં પરિવર્તનને કારણે દ્રષ્ટિની ખોટવાળા બાળકો અને પુખ્ત વયના લોકોની સારવાર માટે પરંતુ પર્યાપ્ત સંખ્યામાં સક્ષમ રેટિના કોષો સાથે.
રિમાર્કસ: Luxturna એ AAV-આધારિત જનીન ઉપચાર છે જે સબરેટિનલ ઇન્જેક્શન દ્વારા સંચાલિત થાય છે.જીન થેરાપી દર્દીના રેટિના કોષોમાં સામાન્ય RPE65 જનીનની કાર્યાત્મક નકલ દાખલ કરવા માટે વાહક તરીકે AAV2 નો ઉપયોગ કરે છે, જેથી સંબંધિત કોષો દર્દીના RPE65 પ્રોટીનની ખામીને સરભર કરવા માટે સામાન્ય RPE65 પ્રોટીનને વ્યક્ત કરે છે, જેનાથી દર્દીની દ્રષ્ટિ સુધરે છે.
(7) Zolgensma
કંપની: નોવાર્ટિસની પેટાકંપની AveXis દ્વારા વિકસિત.
માર્કેટ માટેનો સમય: મે 2019 માં FDA દ્વારા મંજૂર.
સંકેતો: સ્પાઇનલ મસ્ક્યુલર એટ્રોફી (સ્પાઇનલ મસ્ક્યુલર એટ્રોફી, એસએમએ) 2 વર્ષથી ઓછી ઉંમરના દર્દીઓની સારવાર.
રિમાર્કસ: Zolgensma એ AAV વેક્ટર પર આધારિત જનીન ઉપચાર છે.આ દવા કરોડરજ્જુની સ્નાયુબદ્ધ કૃશતા માટે વિશ્વમાં માર્કેટિંગ માટે મંજૂર થયેલ એકમાત્ર એક વખતની સારવાર યોજના છે.પાનું, એક સીમાચિહ્નરૂપ પ્રગતિ છે.આ જીન થેરાપી સામાન્ય SMN1 જનીનને નસમાં ઇન્ફ્યુઝન દ્વારા દર્દીઓમાં દાખલ કરવા માટે scAAV9 વેક્ટરનો ઉપયોગ કરે છે, સામાન્ય SMN1 પ્રોટીન ઉત્પન્ન કરે છે, જેનાથી મોટર ચેતાકોષો જેવા અસરગ્રસ્ત કોષોના કાર્યમાં સુધારો થાય છે.તેનાથી વિપરીત, SMA દવાઓ Spinraza અને Evrysdi ને લાંબા સમય સુધી પુનરાવર્તિત ડોઝની જરૂર પડે છે, જેમાં Spinraza ને દર ચાર મહિને કરોડરજ્જુના ઈન્જેક્શન તરીકે આપવામાં આવે છે, અને Evrysdi, દૈનિક મૌખિક દવા.
(8) ડિલિટેક્ટ
કંપની: ડાઇચી સાંક્યો કંપની લિમિટેડ (TYO: 4568) દ્વારા વિકસિત.
માર્કેટ માટેનો સમય: જૂન 2021માં જાપાનના આરોગ્ય, શ્રમ અને કલ્યાણ મંત્રાલય (MHLW) તરફથી શરતી મંજૂરી.
સંકેતો: જીવલેણ ગ્લિઓમાની સારવાર માટે.
રિમાર્કસ: ડેલીટેક્ટ એ વૈશ્વિક સ્તરે મંજૂર થયેલ ચોથું ઓન્કોલિટીક વાયરસ જીન થેરાપી ઉત્પાદન છે અને જીવલેણ ગ્લિઓમાની સારવાર માટે મંજૂર કરાયેલ પ્રથમ ઓન્કોલિટીક વાયરસ ઉત્પાદન છે.ડેલીટેક્ટ એ આનુવંશિક રીતે એન્જિનિયર્ડ હર્પીસ સિમ્પ્લેક્સ વાયરસ પ્રકાર 1 (HSV-1) ઓન્કોલિટીક વાયરસ છે જે ડો. ટોડો અને સાથીદારો દ્વારા વિકસાવવામાં આવ્યો છે.Delytact બીજી પેઢીના HSV-1 ના G207 જીનોમમાં વધારાના ડિલીટ મ્યુટેશનનો પરિચય આપે છે, જે કેન્સર કોષોમાં તેની પસંદગીયુક્ત પ્રતિકૃતિને વધારે છે અને ઉચ્ચ સલામતી પ્રોફાઇલ જાળવી રાખતી વખતે એન્ટિ-ટ્યુમર રોગપ્રતિકારક પ્રતિક્રિયાઓને ઇન્ડક્શન કરે છે.ડેલીટેક્ટ એ પ્રથમ ત્રીજી પેઢીનું ઓન્કોલિટીક HSV-1 છે જે હાલમાં ક્લિનિકલ મૂલ્યાંકનમાં છે.જાપાનમાં ડેલીટેક્ટની મંજૂરી સિંગલ-આર્મ ફેઝ 2 ક્લિનિકલ ટ્રાયલ પર આધારિત હતી.પુનરાવર્તિત ગ્લિઓબ્લાસ્ટોમા ધરાવતા દર્દીઓમાં, ડેલીટેક્ટ એક વર્ષના અસ્તિત્વના પ્રાથમિક અંતિમ બિંદુને મળ્યા હતા, અને પરિણામો દર્શાવે છે કે ડેલીટેક્ટે G207 કરતાં વધુ સારું પ્રદર્શન કર્યું હતું.મજબૂત પ્રતિકૃતિ અને ઉચ્ચ એન્ટિટ્યુમર પ્રવૃત્તિ.સ્તન, પ્રોસ્ટેટ, શ્વાન્નોમા, નાસોફેરિંજલ, હેપેટોસેલ્યુલર, કોલોરેક્ટલ, જીવલેણ પેરિફેરલ નર્વ શીથ ટ્યુમર્સ અને થાઇરોઇડ કેન્સર સહિતના નક્કર ગાંઠના નમૂનાઓમાં આ અસરકારક છે.
(9) અપસ્ટાઝા
કંપની: PTC Therapeutics, Inc. (NASDAQ: PTCT) દ્વારા વિકસિત.
બજાર માટે સમય: જુલાઈ 2022 માં EU દ્વારા મંજૂર.
સંકેત: સુગંધિત L-amino acid decarboxylase (AADC) ની ઉણપ માટે, 18 મહિના અને તેથી વધુ ઉંમરના દર્દીઓની સારવાર માટે મંજૂર.
રિમાર્કસ: Upstaza™ (eladocagene exuparvovec) એ વેક્ટર તરીકે એડેનો-સંબંધિત વાયરસ પ્રકાર 2 (AAV2) નો ઉપયોગ કરીને વિવો જનીન ઉપચાર છે.AADC એન્ઝાઇમ એન્કોડિંગ જનીનમાં પરિવર્તનને કારણે દર્દી રોગગ્રસ્ત છે.AAV2 એ AADC એન્ઝાઇમને એન્કોડ કરતું તંદુરસ્ત જનીન ધરાવે છે.રોગનિવારક અસર આનુવંશિક વળતરના સ્વરૂપમાં પ્રાપ્ત થાય છે.સિદ્ધાંતમાં, એક ડોઝ લાંબા સમય સુધી અસરકારક છે.તે મગજમાં સીધું ઇન્જેક્ટ કરવામાં આવતી પ્રથમ માર્કેટિંગ જીન થેરાપી છે.માર્કેટિંગ અધિકૃતતા તમામ 27 EU સભ્ય રાજ્યો, તેમજ આઇસલેન્ડ, નોર્વે અને લિક્ટેંસ્ટેઇનને લાગુ પડે છે.
(9) રોક્ટેવિયન
કંપની: BioMarin ફાર્માસ્યુટિકલ (BioMarin) દ્વારા વિકસિત.
બજાર માટે સમય: ઓગસ્ટ 2022 માં EU દ્વારા મંજૂર.
સંકેતો: FVIII પરિબળ નિષેધ અને AAV5 એન્ટિબોડી નેગેટિવ ઇતિહાસ વિના ગંભીર હિમોફિલિયા A ધરાવતા પુખ્ત દર્દીઓની સારવાર માટે.
રિમાર્કસ: રોક્ટેવિયન (વાલોક્ટોકોજેન રોક્સાપાર્વોવેક) AAV5 નો વેક્ટર તરીકે ઉપયોગ કરે છે અને માનવ યકૃત-વિશિષ્ટ પ્રમોટર HLP નો ઉપયોગ B ડોમેન કાઢી નાખવા સાથે માનવ કોગ્યુલેશન ફેક્ટર આઠ (FVIII) ની અભિવ્યક્તિ ચલાવવા માટે કરે છે.વેલોક્ટોકોજેન રોક્સપાર્વોવેકના માર્કેટિંગને મંજૂરી આપવાનો યુરોપિયન કમિશનનો નિર્ણય દવાના ક્લિનિકલ ડેવલપમેન્ટ પ્રોગ્રામના એકંદર ડેટા પર આધારિત છે.તેમાંથી, તબક્કો III ક્લિનિકલ ટ્રાયલ GENEr8-1 દર્શાવે છે કે નોંધણી પહેલાંના વર્ષના ડેટાની તુલનામાં, valoctocogene roxaparvovec ના એક જ ઇન્ફ્યુઝન પછી, વિષયોમાં નોંધપાત્ર રીતે ઓછો વાર્ષિક રક્તસ્ત્રાવ દર (ABR), રિકોમ્બિનન્ટ ફેક્ટર VIII (F8) નો ઓછો વારંવાર ઉપયોગ, લોહીની તૈયારીઓમાં પ્રોટીન પ્રવૃત્તિમાં નોંધપાત્ર વધારો અથવા F8.સારવારના 4 અઠવાડિયા પછી, વિષયોનો વાર્ષિક F8 ઉપયોગ અને સારવારની આવશ્યકતા ધરાવતા ABRમાં અનુક્રમે 99% અને 84% ઘટાડો થયો હતો, જે આંકડાકીય રીતે નોંધપાત્ર તફાવત હતો (p<0.001).સલામતી રૂપરેખા અનુકૂળ હતી, જેમાં કોઈ પણ વિષય F8 પરિબળ નિષેધ, જીવલેણતા, અથવા થ્રોમ્બોટિક આડઅસરનો અનુભવ કરતો ન હતો અને સારવાર સંબંધિત કોઈ ગંભીર પ્રતિકૂળ ઘટનાઓ (SAEs) નોંધવામાં આવી ન હતી.
3. નાના ન્યુક્લીક એસિડ દવાઓ
(1) વિત્રવેણ
કંપની: આયોનિસ ફાર્મા (અગાઉ Isis ફાર્મા) અને નોવાર્ટિસ દ્વારા સંયુક્ત રીતે વિકસિત.
માર્કેટ માટેનો સમય: 1998 અને 1999માં FDA અને EU EMA દ્વારા મંજૂર.
સંકેતો: HIV-પોઝિટિવ દર્દીઓમાં સાયટોમેગાલોવાયરસ રેટિનાઇટિસની સારવાર માટે.
રિમાર્કસ: વિટ્રાવેન એ એન્ટિસેન્સ ઓલિગોન્યુક્લિયોટાઇડ દવા છે અને વિશ્વમાં માર્કેટિંગ માટે મંજૂર કરાયેલ પ્રથમ ઓલિગોન્યુક્લિયોટાઇડ દવા છે.બજારની શરૂઆતમાં, એન્ટિ-સાયટોમેગાલોવાયરસ દવાઓની બજારની માંગ ખૂબ જ તાકીદની હતી;પછી અત્યંત સક્રિય એન્ટિરેટ્રોવાયરલ થેરાપીના વિકાસને કારણે, સાયટોમેગાલોવાયરસના કેસોની સંખ્યામાં તીવ્ર ઘટાડો થયો.બજારની નીચી માંગને કારણે, દવાને 2002 અને 2006 માં EU દેશો અને યુએસમાં ઉપાડ કરવામાં આવી હતી.
(2) મેક્યુજેન
કંપની: Pfizer અને Eyetech દ્વારા સહ-વિકસિત.
માર્કેટ માટેનો સમય: 2004માં યુનાઇટેડ સ્ટેટ્સમાં લિસ્ટિંગ માટે મંજૂર.
સંકેતો: નિયોવાસ્ક્યુલર વય-સંબંધિત મેક્યુલર ડિજનરેશનની સારવાર માટે.
રિમાર્કસ: મેક્યુજેન એ પેજીલેટેડ મોડિફાઇડ ઓલિગોન્યુક્લિયોટાઇડ દવા છે જે વેસ્ક્યુલર એન્ડોથેલિયલ ગ્રોથ ફેક્ટર (વીઇજીએફ165 આઇસોફોર્મ) ને લક્ષ્ય બનાવી શકે છે અને તેને બાંધી શકે છે, અને ઇન્ટ્રાવિટ્રીયલ ઇન્જેક્શન દ્વારા સંચાલિત થાય છે.
(3) ડેફિટેલિયો
કંપની: જાઝ દ્વારા વિકસિત.
માર્કેટ માટેનો સમય: 2013માં યુરોપિયન યુનિયન દ્વારા મંજૂર કરવામાં આવ્યો અને માર્ચ 2016માં FDA દ્વારા મંજૂર કરવામાં આવ્યો.
સંકેતો: હેમેટોપોએટીક સ્ટેમ સેલ ટ્રાન્સપ્લાન્ટેશન પછી રેનલ અથવા પલ્મોનરી ડિસફંક્શન સાથે સંકળાયેલ હેપેટિક વેન્યુલ અવરોધક રોગની સારવાર માટે.
રિમાર્કસ: ડેફિટેલિયો એ ઓલિગોન્યુક્લિયોટાઇડ દવા છે, જે પ્લાઝમિન ગુણધર્મો સાથે ઓલિગોન્યુક્લિયોટાઇડ્સનું મિશ્રણ છે.તેને 2009માં વ્યાપારી કારણોસર પાછી ખેંચી લેવામાં આવી હતી.
(4) Kynamro
કંપની: Ionis Pharma અને Kastle દ્વારા સહ-વિકસિત.
બજાર માટેનો સમય: યુનાઇટેડ સ્ટેટ્સમાં 2013 માં અનાથ દવા તરીકે મંજૂર.
સંકેતો: હોમોઝાયગસ ફેમિલીઅલ હાયપરકોલેસ્ટેરોલેમિયાની સહાયક સારવાર માટે.
રિમાર્કસ: Kynamro એ એન્ટિસેન્સ ઓલિગોન્યુક્લિયોટાઇડ દવા છે, જે માનવ apo B-100 mRNA ને લક્ષ્ય બનાવતી એન્ટિસેન્સ ઓલિગોન્યુક્લિયોટાઇડ છે.Kynamro અઠવાડિયામાં એકવાર 200 મિલિગ્રામ સબક્યુટેનલી તરીકે આપવામાં આવે છે.
(5) સ્પિનરાઝા
કંપની: આયોનિસ ફાર્માસ્યુટિકલ્સ દ્વારા વિકસિત.
માર્કેટ માટેનો સમય: ડિસેમ્બર 2016 માં FDA દ્વારા મંજૂર.
સંકેતો: સ્પાઇનલ મસ્ક્યુલર એટ્રોફી (SMA) ની સારવાર માટે.
રિમાર્કસ: સ્પિનરાઝા (નુસિનરસેન) એ એન્ટિસેન્સ ઓલિગોન્યુક્લિયોટાઇડ દવા છે.સ્પિનરાઝા SMN2 એક્સોન 7 ની સ્પ્લિસિંગ સાઇટ સાથે જોડાઈને SMN2 જનીનનું RNA સ્પ્લિસિંગ બદલી શકે છે, જેનાથી સંપૂર્ણ કાર્યકારી SMN પ્રોટીનનું ઉત્પાદન વધે છે.ઓગસ્ટ 2016 માં, BIOGEN કોર્પોરેશને સ્પિનરાઝાના વૈશ્વિક અધિકારો પ્રાપ્ત કરવા માટે તેના વિકલ્પનો ઉપયોગ કર્યો.સ્પિનરાઝાએ 2011 માં મનુષ્યો પર તેની પ્રથમ ક્લિનિકલ ટ્રાયલ શરૂ કરી હતી. માત્ર 5 વર્ષમાં, તેને 2016 માં FDA દ્વારા મંજૂર કરવામાં આવ્યું હતું, જે FDA દ્વારા તેની અસરકારકતાની સંપૂર્ણ માન્યતાને પ્રતિબિંબિત કરે છે.આ દવાને એપ્રિલ 2019માં ચીનમાં માર્કેટિંગ માટે મંજૂર કરવામાં આવી હતી. ચીનમાં સ્પિનરાઝાની સંપૂર્ણ મંજૂરી ચક્ર 6 મહિનાથી પણ ઓછું છે.યુનાઇટેડ સ્ટેટ્સમાં સ્પિનરાઝાને પ્રથમ વખત મંજૂર થયાને 2 વર્ષ અને 2 મહિના થયા છે.આવી બ્લોકબસ્ટર વિદેશી દુર્લભ બીમારીની નવી દવા ચીનમાં લિસ્ટિંગની ઝડપ પહેલેથી જ ખૂબ જ ઝડપી છે.આ 1 નવેમ્બર, 2018 ના રોજ સેન્ટર ફોર ડ્રગ ઈવેલ્યુએશન દ્વારા જારી કરાયેલ "ઓવરસીઝ નવી દવાઓની ફર્સ્ટ લિસ્ટ ઓફ ધ રીલીઝ ઓન ધ નોટિસ ઓન ધ રીલીઝ ઓફ અર્જન્ટલી નીડ ફોર ક્લિનિકલ રિસર્ચ" ને કારણે પણ છે, જે ઝડપી સમીક્ષા માટે 40 કી વિદેશી નવી દવાઓની પ્રથમ બેચમાં સામેલ હતી અને તેમાં સ્પિનરાઝાને સ્થાન આપવામાં આવ્યું હતું.
(6) એક્સોન્ડિસ 51
કંપની: AVI બાયોફાર્મા દ્વારા વિકસિત (પછીથી સારેપ્ટા થેરાપ્યુટિક્સ નામ આપવામાં આવ્યું).
બજાર માટેનો સમય: સપ્ટેમ્બર 2016 માં FDA દ્વારા મંજૂર.
સંકેતો: એક્સોન 51 સ્કિપિંગ જનીનમાં ડીએમડી જનીન પરિવર્તન સાથે ડ્યુચેન મસ્ક્યુલર ડિસ્ટ્રોફી (ડીએમડી) ની સારવાર માટે.
રિમાર્કસ: Exondys 51 એ એન્ટિસેન્સ ઓલિગોન્યુક્લિયોટાઇડ દવા છે.એન્ટિસેન્સ ઓલિગોન્યુક્લિયોટાઇડ DMD જનીનની પૂર્વ-mRNA ની એક્ઝોન 51 સ્થિતિ સાથે જોડાઈ શકે છે, પરિણામે પરિપક્વ mRNA ની રચના થાય છે.આંશિક રીતે એમઆરએનએ રીડિંગ ફ્રેમને સુધારીને એક્સિઝન, દર્દીને સામાન્ય પ્રોટીન કરતાં ટૂંકા હોય તેવા ડિસ્ટ્રોફિનના કેટલાક કાર્યાત્મક સ્વરૂપોને સંશ્લેષણ કરવામાં મદદ કરે છે, જેનાથી દર્દીના લક્ષણોમાં સુધારો થાય છે.
(7) ટેગસેડી
કંપની: આયોનિસ ફાર્માસ્યુટિકલ્સ દ્વારા વિકસિત.
માર્કેટિંગ માટેનો સમય: જુલાઈ 2018 માં માર્કેટિંગ માટે યુરોપિયન યુનિયન દ્વારા મંજૂર.
સંકેતો: વારસાગત ટ્રાન્સથાયરેટિન એમાયલોઇડિસિસ (એચએટીટીઆર) ની સારવાર માટે.
રિમાર્કસ: ટેગસેડી એ એન્ટિસેન્સ ઓલિગોન્યુક્લિયોટાઇડ દવા છે જે ટ્રાંસથાયરેટિન એમઆરએનએને લક્ષ્ય બનાવે છે.HATTR ની સારવાર માટે તે વિશ્વની પ્રથમ માન્ય દવા છે.વહીવટની પદ્ધતિ સબક્યુટેનીયસ ઇન્જેક્શન છે.આ દવા ટ્રાંસથાયરેટિન (ATTR) ના mRNA ને લક્ષ્ય બનાવીને ATTR પ્રોટીનનું ઉત્પાદન ઘટાડે છે, અને ATTR ની સારવારમાં સારો લાભ-જોખમ ગુણોત્તર ધરાવે છે.ન તો રોગનો તબક્કો કે કાર્ડિયોમાયોપેથીની હાજરી સંબંધિત ન હતી.
(8) ઓનપેટ્રો
કંપની: Alnylam અને Sanofi દ્વારા સહ-વિકસિત.
માર્કેટ માટેનો સમય: 2018 માં યુનાઇટેડ સ્ટેટ્સમાં સૂચિબદ્ધ કરવા માટે મંજૂર.
સંકેતો: વારસાગત ટ્રાન્સથાયરેટિન એમાયલોઇડિસિસ (એચએટીટીઆર) ની સારવાર માટે.
રિમાર્કસ: ઓનપેટ્રો એ ટ્રાન્સથાયરેટિન એમઆરએનએને લક્ષ્યાંકિત કરતી siRNA દવા છે, જે યકૃતમાં ATTR પ્રોટીનનું ઉત્પાદન ઘટાડે છે અને ટ્રાન્સથાયરેટિન (ATTR) ના mRNA ને લક્ષ્ય બનાવીને પેરિફેરલ ચેતામાં એમીલોઇડ થાપણોના સંચયને ઘટાડે છે., ત્યાંથી રોગના લક્ષણોમાં સુધારો અને રાહત.
(9) Givlaari
કંપની: Alnylam કોર્પોરેશન દ્વારા વિકસિત.
માર્કેટ માટેનો સમય: નવેમ્બર 2019 માં FDA દ્વારા મંજૂર.
સંકેતો: પુખ્ત વયના લોકોમાં તીવ્ર હિપેટિક પોર્ફિરિયા (એએચપી) ની સારવાર માટે.
રિમાર્કસ: Givlaari એ siRNA દવા છે, જે Onpattro પછી માર્કેટિંગ માટે મંજૂર થયેલ બીજી siRNA દવા છે.દવા સબક્યુટેનીયસ રીતે આપવામાં આવે છે અને ALAS1 પ્રોટીનના અધોગતિ માટે mRNA ને લક્ષ્ય બનાવે છે.માસિક Givlaari સારવાર યકૃતમાં ALAS1 ના સ્તરને નોંધપાત્ર રીતે અને સતત ઘટાડી શકે છે, ત્યાં ન્યુરોટોક્સિક ALA અને PBG ના સ્તરને સામાન્ય શ્રેણીમાં ઘટાડે છે, જેથી દર્દીના રોગના લક્ષણોમાં રાહત મળે છે.ડેટા દર્શાવે છે કે ગીવલારીની સારવાર કરાયેલા દર્દીઓમાં પ્લેસબો જૂથની તુલનામાં રોગના જ્વાળાઓની સંખ્યામાં 74% ઘટાડો થયો હતો.
(10) વ્યોન્ડિસ53
કંપની: સારેપ્ટા થેરાપ્યુટિક્સ દ્વારા વિકસિત.
માર્કેટ માટેનો સમય: ડિસેમ્બર 2019 માં FDA દ્વારા મંજૂર.
સંકેત: ડિસ્ટ્રોફિન જીન એક્સોન 53 સ્પ્લાઈસ મ્યુટેશનવાળા ડીએમડી દર્દીઓની સારવાર માટે.
ટિપ્પણી: Vyondys 53 એ એન્ટિસેન્સ ઓલિગોન્યુક્લિયોટાઇડ દવા છે.ઓલિગોન્યુક્લિયોટાઇડ દવા ડિસ્ટ્રોફિન mRNA પુરોગામીની વિભાજન પ્રક્રિયાને લક્ષ્ય બનાવે છે.ડિસ્ટ્રોફિન mRNA પુરોગામીની પરોક્ષ પ્રક્રિયામાં, બાહ્ય એક્ઝોન 53 આંશિક રીતે વિભાજિત કરવામાં આવ્યું હતું, એટલે કે પરિપક્વ mRNA પર હાજર નથી, અને તેને કપાયેલ પરંતુ હજુ પણ કાર્યરત ડિસ્ટ્રોફિન પ્રોટીન બનાવવા માટે ડિઝાઇન કરવામાં આવ્યું હતું, જેનાથી દર્દીઓમાં કસરત કરવાની ક્ષમતામાં સુધારો થાય છે.
(11) વેલીવ્રા
કંપની: Ionis ફાર્માસ્યુટિકલ્સ અને તેની પેટાકંપની Akcea Therapeutics દ્વારા વિકસિત.
માર્કેટ માટેનો સમય: મે 2019 માં યુરોપિયન મેડિસિન એજન્સી (EMA) દ્વારા મંજૂર.
સંકેત: કૌટુંબિક chylomicronemia સિન્ડ્રોમ (FCS) ધરાવતા પુખ્ત દર્દીઓમાં નિયંત્રિત આહાર માટે સહાયક ઉપચાર તરીકે.
રિમાર્કસ: વેલિવ્રા એ એન્ટિસેન્સ ઓલિગોન્યુક્લિયોટાઇડ દવા છે, જે વિશ્વમાં એફસીએસની સારવાર માટે મંજૂર કરાયેલ પ્રથમ દવા છે.
(12) Leqvio
કંપની: નોવાર્ટિસ દ્વારા વિકસિત.
બજાર માટે સમય: ડિસેમ્બર 2020 માં EU દ્વારા મંજૂર.
સંકેતો: પુખ્ત વયના પ્રાથમિક હાયપરકોલેસ્ટેરોલેમિયા (વિષમ-પારિવારિક અને બિન-પારિવારિક) અથવા મિશ્ર ડિસ્લિપિડેમિયાની સારવાર માટે.
રિમાર્કસ: લેક્વિઓ એ PCSK9 mRNA ને લક્ષ્ય બનાવતી siRNA દવા છે.તે વિશ્વની પ્રથમ કોલેસ્ટ્રોલ-લોઅરિંગ (LDL-C) siRNA ઉપચાર છે.વહીવટની પદ્ધતિ સબક્યુટેનીયસ ઇન્જેક્શન છે.પીસીએસકે 9 પ્રોટીન સ્તરને ઘટાડવા માટે દવા આરએનએ હસ્તક્ષેપ દ્વારા કાર્ય કરે છે, જે બદલામાં એલડીએલ-સી સ્તરને ઘટાડે છે.ક્લિનિકલ ડેટા દર્શાવે છે કે લેક્વિઓ એવા દર્દીઓમાં લગભગ 50% જેટલો LDL-C ઘટાડી શકે છે જેમના LDL-C સ્તરને સ્ટેટિન્સની મહત્તમ સહનશીલ માત્રા હોવા છતાં લક્ષ્ય સ્તર સુધી ઘટાડી શકાતું નથી.
(13) ઓક્સલુમો
કંપની: Alnylam ફાર્માસ્યુટિકલ્સ દ્વારા વિકસિત.
બજાર માટેનો સમય: નવેમ્બર 2020 માં EU દ્વારા મંજૂર.
સંકેતો: પ્રાથમિક હાયપરઓક્સાલુરિયા પ્રકાર 1 (PH1) ની સારવાર માટે.
રિમાર્કસ: ઓક્સલુમો એ હાઇડ્રોક્સી એસિડ ઓક્સિડેઝ 1 (HAO1) mRNA ને લક્ષ્ય બનાવતી siRNA દવા છે, જે સબક્યુટેનીયસ રીતે સંચાલિત થાય છે.દવા Alnylam ની નવીનતમ ઉન્નત સ્થિરીકરણ રસાયણ ESC-GalNAc સંયોજક તકનીકનો ઉપયોગ કરીને વિકસાવવામાં આવી હતી, જે વધુ દ્રઢતા અને અસરકારકતા સાથે સબક્યુટેનલી સંચાલિત siRNA ને સક્ષમ કરે છે.દવા hydroxy acid oxidase 1 (HAO1) mRNA ના અધોગતિ અથવા નિષેધને લક્ષ્ય બનાવે છે, યકૃતમાં ગ્લાયકોલેટ ઓક્સિડેઝનું સ્તર ઘટાડે છે, અને પછી ઓક્સાલેટના ઉત્પાદન માટે જરૂરી સબસ્ટ્રેટનો ઉપયોગ કરે છે અને રોગની પ્રગતિને નિયંત્રિત કરવા અને દર્દીઓમાં રોગના લક્ષણોમાં સુધારો કરવા માટે ઓક્સાલેટનું ઉત્પાદન ઘટાડે છે.
(14) વિલ્ટેપ્સો
કંપની: NS ફાર્મા દ્વારા વિકસિત, નિપ્પોન શિન્યાકુની પેટાકંપની.
માર્કેટ માટેનો સમય: ઓગસ્ટ 2020 માં FDA દ્વારા મંજૂર.
સંકેતો: એક્ઝોન 53 સ્કિપિંગ જનીનમાં ડીએમડી જનીન પરિવર્તન સાથે ડ્યુચેન મસ્ક્યુલર ડિસ્ટ્રોફી (ડીએમડી) ની સારવાર માટે.
ટિપ્પણીઓ: વિલ્ટેપ્સો એ ફોસ્ફોરોડિયામાઇડ મોર્ફોલિનો ઓલિગોન્યુક્લિયોટાઇડ દવા છે.આ ઓલિગોન્યુક્લિયોટાઇડ દવા DMD જનીનની પૂર્વ-mRNA ની exon 53 સ્થિતિ સાથે જોડાઈ શકે છે, પરિણામે પરિપક્વ mRNA ની રચના થાય છે.એક્ઝોન આંશિક રીતે દૂર કરવામાં આવે છે, આમ mRNA રીડિંગ ફ્રેમને આંશિક રીતે સુધારે છે, દર્દીને ડિસ્ટ્રોફિનના કેટલાક કાર્યાત્મક સ્વરૂપોને સંશ્લેષણ કરવામાં મદદ કરે છે જે સામાન્ય પ્રોટીન કરતા ટૂંકા હોય છે, જેથી દર્દીના લક્ષણોમાં સુધારો થાય છે.
(15) અમવુત્ર (વ્યુત્રિસિરન)
કંપની: Alnylam ફાર્માસ્યુટિકલ્સ દ્વારા વિકસિત.
બજાર માટેનો સમય: FDA દ્વારા જૂન 2022 માં મંજૂર.
સંકેતો: પોલિન્યુરોપથી (hATTR-PN) સાથે પુખ્ત વારસાગત ટ્રાંસથાઇરેટિન એમાયલોઇડિસિસની સારવાર માટે.
ટિપ્પણીઓ: Amvuttra (Vutrisiran) એ siRNA દવા છે જે ટ્રાંસથાયરેટિન (ATTR) mRNA ને લક્ષ્ય બનાવે છે, જે સબક્યુટેનીયસ ઈન્જેક્શન દ્વારા સંચાલિત થાય છે.Vutrisiran એ Alnylam ના ઉન્નત સ્થિરીકરણ રસાયણશાસ્ત્ર (ESC)-GalNAc કન્જુગેટેડ ડિલિવરી પ્લેટફોર્મ પર આધારિત છે જેમાં વધેલી શક્તિ અને મેટાબોલિક સ્થિરતા છે.થેરાપીની મંજૂરી તેના ત્રીજા તબક્કાના ક્લિનિકલ અભ્યાસ (HELIOS-A) ના 9-મહિનાના ડેટા પર આધારિત છે, એકંદર પરિણામો દર્શાવે છે કે ઉપચારથી hATTR-PN ના લક્ષણોમાં સુધારો થયો છે, 50% થી વધુ દર્દીઓ પ્રગતિને ઉલટાવી રહ્યા છે અથવા રોકે છે.
4. અન્ય જનીન ઉપચાર દવાઓ
(1) રેક્સિન-જી
કંપની: Epeius બાયોટેક દ્વારા વિકસિત.
બજાર માટેનો સમય: 2005 માં ફિલિપાઈન ફૂડ એન્ડ ડ્રગ એડમિનિસ્ટ્રેશન (BFAD) દ્વારા મંજૂર.
સંકેતો: અદ્યતન કેન્સરની સારવાર માટે જે કીમોથેરાપી માટે પ્રતિરોધક છે.
રિમાર્કસ: રેક્સિન-જી એ જીન-લોડેડ નેનોપાર્ટિકલ ઈન્જેક્શન છે.તે ખાસ કરીને નક્કર ગાંઠોને મારવા માટે રેટ્રોવાયરલ વેક્ટર દ્વારા લક્ષ્ય કોષોમાં સાયક્લિન G1 મ્યુટન્ટ જનીન દાખલ કરે છે.વહીવટની પદ્ધતિ નસમાં પ્રેરણા છે.ટ્યુમર-લક્ષિત દવા તરીકે જે મેટાસ્ટેટિક કેન્સર કોષોને સક્રિય રીતે શોધે છે અને તેનો નાશ કરે છે, તે એવા દર્દીઓ પર ચોક્કસ અસર કરે છે કે જેઓ લક્ષિત જીવવિજ્ઞાન સહિત અન્ય કેન્સરની દવાઓ સામે બિનઅસરકારક છે.
(2) Neovasculgen
કંપની: માનવ સ્ટેમ સેલ સંસ્થા દ્વારા વિકસિત.
લિસ્ટિંગનો સમય: 7 ડિસેમ્બર, 2011ના રોજ રશિયામાં લિસ્ટિંગ માટે મંજૂર, અને પછી 2013માં યુક્રેનમાં સૂચિબદ્ધ.
સંકેતો: ગંભીર અંગ ઇસ્કેમિયા સહિત પેરિફેરલ ધમની બિમારીની સારવાર માટે.
રિમાર્કસ: નિયોવાસ્ક્યુલજેન એ ડીએનએ પ્લાઝમિડ-આધારિત જનીન ઉપચાર છે જેમાં વેસ્ક્યુલર એન્ડોથેલિયલ ગ્રોથ ફેક્ટર (VEGF) 165 જનીન પ્લાઝમિડ બેકબોન પર બાંધવામાં આવે છે અને દર્દીઓમાં દાખલ કરવામાં આવે છે.
(3) કોલેટજીન
કંપની: ઓસાકા યુનિવર્સિટી અને વેન્ચર કેપિટલ કંપનીઓ દ્વારા સહ-વિકસિત.
લિસ્ટિંગનો સમય: ઑગસ્ટ 2019માં લિસ્ટિંગ માટે જાપાનના આરોગ્ય, શ્રમ અને કલ્યાણ મંત્રાલય દ્વારા મંજૂર.
સંકેતો: ગંભીર નીચલા હાથપગના ઇસ્કેમિયાની સારવાર.
રિમાર્કસ: કોલેટજીન એ પ્લાઝમિડ-આધારિત જનીન ઉપચાર છે, જે એન્જીસ દ્વારા ઉત્પાદિત પ્રથમ મૂળ જાપાની જનીન ઉપચાર દવા છે.આ દવાનો મુખ્ય ઘટક નગ્ન પ્લાઝમિડ છે જેમાં માનવ હેપેટોસાઇટ વૃદ્ધિ પરિબળ (HGF) ના જનીન ક્રમ છે.જો દવાને નીચલા અંગોના સ્નાયુઓમાં ઇન્જેક્ટ કરવામાં આવે છે, તો વ્યક્ત HGF અવરોધિત રક્ત વાહિનીઓની આસપાસ નવી રક્ત વાહિનીઓના નિર્માણને પ્રોત્સાહન આપશે.ક્લિનિકલ ટ્રાયલોએ અલ્સરને સુધારવામાં તેની અસરકારકતાની પુષ્ટિ કરી છે.
અંત
પોસ્ટ સમય: નવેમ્બર-10-2022